|
||||
細胞内の1分子の動きの超精密測定などの最先端かつ日本オリジナルの計測技術をさらに高度化し、細胞・組織における生体分子(mRNA・タンパク質・イオン分子等)の発現量などの化学的特性、および分子情報・力学・電場等の特性について、その時間的・空間的変化を定量的に計測するための手法を開発する。 これにより、「細胞内分子動態イメージング法」「1細胞分子検出法」「組織・器官内の1細胞解析法」を実現する。 これらの技術を基に、細胞内の複雑な反応ネットワーク・力学応答の動態の特徴を数値データとして取得し、統計解析・数理モデル構築・大規模シミュレーション・摂動計算等を通して、細胞動態の制御原理の解明を目指す。 |
||||
生体運動を司る分子モーターの直接計測や細胞膜上の受容体の可視化など、日本は世界に先けて水溶液中における生きたタンパク質の1分子可視化・計測技術を発展させてきた。 このユニークな技術をさらに発展させ、細胞内情報伝達系や組織・器官など生体システムがダイナミックに機能している場における分子の時空間的な動態の計測を可能にする「細胞内分子動態イメージング法」の開発を進める。このためには、以下を実現する必要がある。 • 細胞内でのナノメータ空間分解能およびミリ秒時間分解能の実現 • 生きた細胞・組織内での分子の3次元分布・動態計測 • 広帯域マルチカラーイメージングによる多種分子間相互作用の同時計測 このような計測により、細胞内での遺伝子発現の可視化 、刺激に反応している細胞の膜上における 受容体分子の時空間分布や細胞骨格・細胞の極性の時間変化、興奮時の膜電位・静電相互作用、 免疫反応などの高次生体反応を定量的に計測できると期待される。 これらを実現するため、要素技術として光源・検鏡法・プローブについて集中的に開発する。 |
  |
|||
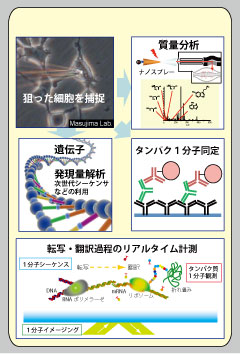
最先端計測技術と、組織内の特定の細胞1個を捕捉・操作する技術とを融合することにより、細胞に刺激を加えた後の動態変化の瞬間の細胞内成分を網羅的に分析することが可能になる。 例えば、ナノスプレー技術を用いた1細胞質量分析法により、細胞顆粒内の様々な代謝物も含めた生合成の様子が、短時間でモニター可能となっている。また、抗体によるより感度の高いタンパク質同定、次世代シーケンサによる 遺伝子発現量の計測においても、1細胞レベルでの計測は実現可能である。 これらと前述の一分子動態計測などの組み合わせにより、関係分子群の質や量の変化・動きを同時に追跡し、細胞活動全体の把握を目指す。さらに、生きた細胞あるいは再構成系での動態計測の実現に向け、転写過程におけるmRNA 分子の動態やタンパク質の発現過程をリアルタイムで連続観察することにより、 mRNA の1分子単位での塩基配列計測や、タンパク質-タンパク質・リガンド相互作用過程の追跡を可能にすることを目指す。 |
 |
|||
現在iPS細胞に代表される再生医学分野の発展には目覚ましいものがあり、1日も早い臨床応用の期待が高い。 しかし、細胞分化の多能性の獲得メカニズムにはまだ不明な点もあり、完全に安全な臨床応用にはさらなる 知見の蓄積が必要な状況である。幹細胞がある特定の機能を持つ細胞に分化し、 さらに周囲の細胞とネットワークを形成してより高次の機能を持つシステムを形づくる際の細胞や細胞内分子の動態を連続的に計測することは、生体機能発現の動態を理解しそれを制御する上で非常に重要である。 前述の細胞内分子動態イメージング技術、1細胞分子検出技術、その他の技術を組み合わせることにより、 多細胞体での個々の細胞動態の連続計測の実現を目指す。このためには特に組織の深部に対する 非侵襲の計測や、3+1次元での遺伝子発現量・タンパク質発現量の計測を、極力1細胞を分解できるような スケールで実現することが望まれる。本技術は細胞の状態を制御する原理の解明に繋がるとともに、 生命科学の広い分野に適用可能であり、世界的な研究競争でリードを奪うための基盤的な技術となりうる。 |
||||
| |このページの先頭へ↑| | ||||

