TOP > ニュース・特集 > 体内時計が温度に依存しない仕組みを原子レベルで解明
細菌からヒトまでほとんどの生物種には、約24時間の周期で繰り返される体内時計が備わっています。体内時計には、光などの外部環境を遮断しても自律的に約24時間周期で変動する、外部環境の変化に対して同調できるという性質のほか、周期が温度に依存せず常に一定である「温度補償性」という特徴があります。
2009年に理研の研究チームは、哺乳類の体内時計の周期長を決定しているのは、リン酸化酵素カゼインキナーゼⅠδ(CKⅠδ)によるリン酸化反応であることを発見しました。さらに、一般的な生体内の生化学反応は温度が10℃上がると、反応速度は2~3倍速くなるのに対して、CKⅠδによるリン酸化反応は温度に依存せずに一定でした。この結果から、CKⅠδのリン酸化反応と温度補償性との関係性を示しました。しかし、その詳しい反応機構は明らかになっていません。
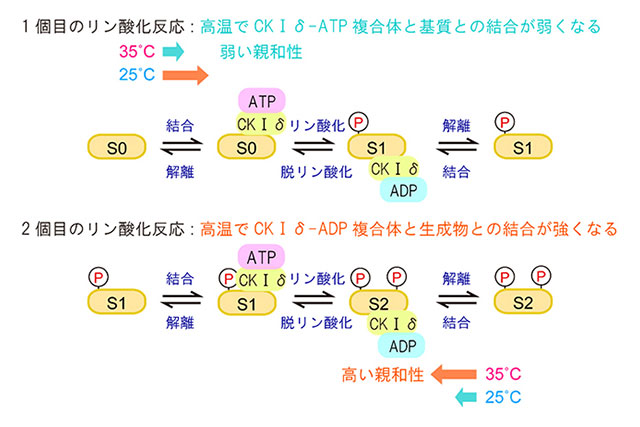
今回、理研を中心とする共同研究グループは、生化学実験と実験データに基づいた数理モデルにより、「CKⅠδ-ATP複合体と基質との結合が高温で弱くなること」と「CKⅠδ-ADP複合体と生成物との結合が高温で強くなること」の二つの結合メカニズムが、高温に伴う反応速度の上昇にブレーキをかけ、その結果として、温度に依存しないリン酸化反応を実現していることを解明しました(図参照)。また、アウリントリカルボン酸という低分子化合物とCKⅠδ変異体による遺伝学的アプローチによる検証実験を行い、温度補償性には温度依存的な生成物結合が重要であることが分かりました。さらに、ヒト由来の温度依存的なリン酸化酵素TTBK1にCKⅠファミリー固有の領域を挿入することで、温度に依存しないリン酸化反応を「創る」ことに成功しました。
本成果は、約60年間にわたって謎とされてきた温度補償性の分子機構を明らかにしたもので、体内時計研究を大きく進展させるものです。また、本研究で発見した低分子化合物や、体内時計の周期を短くするCKⅠδ変異体は、概日リズム睡眠障害などのメカニズムの解明や薬剤による治療法の開発にも貢献すると期待できます。
- Y. Shinohara, Y. M. Koyama, M. Ukai-Tadenuma, et al. "Temperature-sensitive substrate and product binding underlie temperature-compensated phosphorylation in the clock", Molecular Cell, in press


