- 1
自発的細胞内極性形成
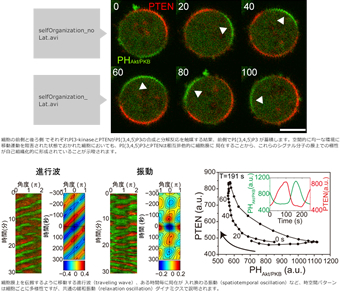
細胞の自発的な極性形成と運動
細胞は一定な環境においてもランダムに方向転換を繰り返しながら移動運動を行います。細胞の前後極性の自発的な形成には、イノシトールリン脂質代謝系の自己組織化反応が関わっていることが明らかになっています。確率的に動作する生体分子の集まりからどのようにして極性シグナルが生成されるのか、また、基質との接着などの他のシグナル伝達系からどのような制御を受けて効率的な運動が行われるのか、という問いに中心的に取り組み、細胞の自発性の起源と発現メカニズムを理解することを目指しています。
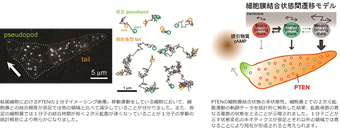
自己組織化による局在形成過程の1分子イメージング解析
イノシトールリン脂質の自己組織化に欠かせない代謝酵素であるPTENは、細胞質と細胞膜との間を行き来しながらPtdIns(3‚4‚5)P3の脱リン酸化を触媒します。そこで、PTENの細胞膜との結合、細胞膜上での酵素反応と結合状態の変化、細胞膜からの解離のそれぞれの動的特性を明らかにするために、1分子イメージングによって生きた細胞でのPTEN分子の運動・反応を解析しています。分子生物学的・生化学的・構造生物学的手法も採り入れ、確率的な分子同士の相互作用を通して自律的に局在が形成されるメカニズムを解明することを目指します。
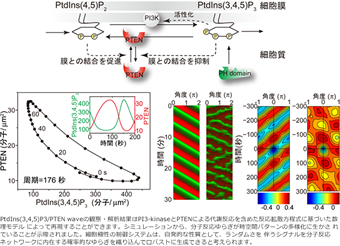
数理モデルシミュレーションによるダイナミクスの再現
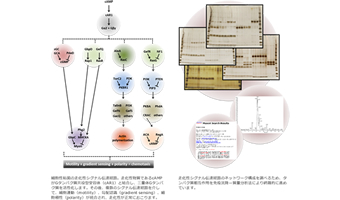
ライブセルマルチカラーイメージングや1分子イメージングによって分子集団の挙動や1分子の反応・運動を精密計測し、得られたデータの統計解析によって平均的なダイナミクスと確率的な特性を明らかにできます。こうした定量的データとシステムの振る舞いに対する理解を繋ぐ上で、数理モデルは非常に強力なツールとなります。計測結果に基づいたモデル構築、モデルのシミュレーションによる現象の再現、予測された事象の実験による検証、というように実験計測とモデル化の繰り返しを通して、自己組織化メカニズムの解明を試みています。
- 2
シグナル伝達とセンシング
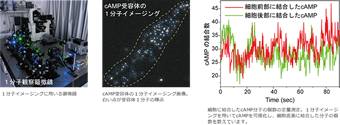
cAR1受容体の1分子イメージング
細胞性粘菌の走化性シグナル伝達は、細胞膜上にあるGPCR型cAMP受容体(cAR1と呼ばれる)によって媒介されています。このとき粘菌細胞は細胞両端でのcAMP濃度の高低、すなわちcAMPの受容体への結合数の違いを検知しています。cAMPと受容体の結合・解離反応は確率的であるために、活性化型受容体の数は時間的に一定せず、平均値の周りでゆらぎます。この平均値をcAMP濃度に対応したシグナルと考えると、そのゆらぎは濃度情報の読み取り誤差であり、シグナルをあいまいにするノイズだと言えます。粘菌細胞が走化性を示す条件下では、このノイズが走化性シグナルと同程度かそれを上回っていることが予想されます。このような条件下でも走化性を示す細胞性粘菌は、どのようなシグナル伝達を行っているのでしょうか。1分子イメージングを用いることで、細胞へのシグナルやノイズを可視化し、それらを定量的に解析することができます。
ErbB受容体によるシグナル伝達の調節機構
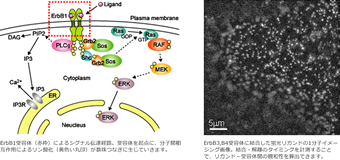
細胞膜に局在し、細胞外からのシグナルを細胞内に伝達するErbB受容体はErbB1からErbB4までの4種類から構成され、それぞれに特異的なリガンドが知られています。細胞内のシグナル伝達経路も受容体ごとに異なっているため、リガンド-受容体の組み合わせによって細胞の応答も変わってきます。例えば、上皮成長因子(Epidermal Growth factor, EGF)をリガンドとするErbB1は、EGF受容体(EGF receptor, EGFR)とも呼ばれ、主に細胞増殖に関与しています。そのため、ErbB1の発現量の調節が出来なくなったり、変異によって機能が損なわれると、細胞の増殖に異常をきたし癌など重篤な疾病の原因となります。
蛍光プローブを結合させたErbB分子の1分子イメージングにより、細胞膜上の個々の受容体を直接観察することができます。得られた画像中の蛍光輝点の運動軌跡や蛍光強度を解析することで、分子動態やリガンドとの相互作用、他のシグナル伝達分子との反応に関する詳細な情報が得られます。私達はこれらの情報を基にシグナル伝達の調節機構を理解し、細胞応答が決定されるプロセスをはじめ、疾病の発症や進行のメカニズムを明らかにすることを目指しています。
情報処理タンパク質RAS、RAFの1分子イメージングと細胞の運命決定
細胞は、外部の環境や内部の状態に依存して、増殖、分化、運動、ガン化、死など、様々な運命をたどります。これら細胞運命の決定機構を理解し、細胞応答の予測および操作を実現することは、再生医療やガン治療の発展の基礎となる重要な課題の1つです。
私たちは、増殖、分化、ガン化などの細胞の運命を左右する重要な反応の1つ「情報処理タンパク質RASからRAFへの反応」に注目して、細胞内情報伝達反応に重要なタンパク質の構造分布や構造変化、タンパク質間相互作用、リン酸化や脱リン酸化などの酵素反応の時空間ダイナミクスを、細胞内1分子検出技術を駆使してしらべ、RASからRAFへの情報処理反応が細胞の運命決定機構にとどのように関わっているかを明らかにすることを目指しています。
免疫細胞におけるインテグリン1分子イメージング
細胞が生体内で接着移動するのに重要な役割を担っているタンパク質の一つにインテグリン分子があります。このインテグリンが免疫系ではどのように働いてリンパ球の接着移動を制御しているのかを解明するため、インテグリンやそれと相互作用する分子の動態を1分子イメージングすることにより解析しています。免疫細胞動態の制御機構を解明することは免疫システムの操作につながり、医療において新しい戦略を提供することが期待されます。
走化性におけるシグナリングネットワーク
細胞は外界の化学物質を感知し、誘因あるいは忌避運動を示します。このような現象は走化性と呼ばれ、胚発生、脳における神経のパターン形成、がん細胞の原発巣からの転移など多くの場面で観察されます。我々は細胞が化学物質の濃度勾配を認識し、方向性のある運動へ変換するしくみを知るため、走化性を構成する因子と機能モジュールの同定を進めると共に、それらの反応ダイナミクスを定量的に明らかにしようと試みています。このような研究は 生物システムがもつ情報処理のしなやかさを理解し、工学、医学分野に応用可能な基盤技術へとつながることが期待されます。
転写のゆらぎ
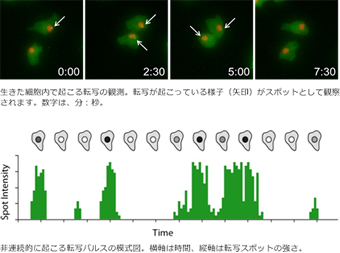
DNAの情報からRNAが作られる転写は、生細胞内でのRNA産生を直接観測する革新的な技術により、不規則な長さや強さで起こるバースト状(パルス状)であることが明らかになっています。私達は、このバースト状に発生する転写の基本メカニズム、および発生分化過程でのシグナルへの応答性やクロマチン構造の影響などの理解を目指しています。さらに、ここで見られる転写のゆらぎと細胞分化などで見られる多様性との関わりあいの理解も試みています。
- 3
定量計測技術開発
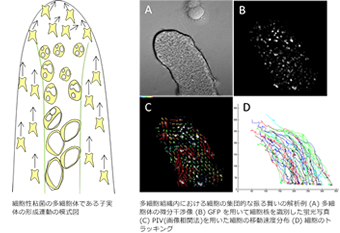
多細胞組織内における細胞のトラッキング
一個一個ばらばらだった細胞は集合して多細胞組織を作り出します。細胞の集団的な振る舞い(collective migration)を解析することで、秩序だった組織を形成するメカニズムの解明を目指します。これらの研究は多細胞動物において組織を形成する原理の解明につながり、再生医療への応用が期待されます。
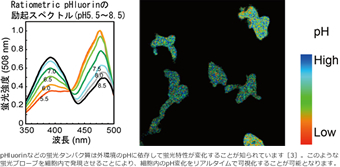
細胞内pHイメージング
細胞内pHは細胞のシグナル伝達において重要な要因の一つとして働いていることが示唆されています。例えば、細胞の運動速度と細胞内pH には高い相関があることが知られています[1‚2]。細胞内pHのシグナル伝達における役割を解明するため、生細胞の細胞内pHイメージングを行うことにより、解析を行っています。また、細胞のがん化によって細胞内pHが変化することが知られており、細胞内pHが細胞内シグナル伝達においてどのように働いているかを解明することは、医療の発展に極めて重要な情報を得ることが期待されます。
References- [1]
- Simchowitz L. & Cragoe E. J. Jr. J. Biol. Chem. 261‚ 6492-6500. (1986)
- [2]
- Van Duijn B. & Inouye‚ K. PNAS 88‚ 4951?4955 (1991).
- [3]
- Miesenbock G‚ et al.‚ Nature 394‚ 192?195‚ (1998).
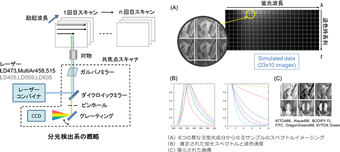
マルチカラーイメージング
蛍光顕微鏡法の多色化は共同的に働く細胞内コンポーネントを解析する上で極めて重要であると考えられます。この目的のために様々な蛍光色素や蛍光タンパクが開発されつつありますが、これを観察するための蛍光顕微鏡法としては6色程度が上限であり、4色以上の同時イメージングを実用的に行う例は極めてまれです。原理的には、分光を用いたスペクトルイメージングとリニアアンミキシング法を用いれば10色以上の同時イメージングが可能ですが、各色素ごとに単染色のリファレンスサンプルを用意しなければならなかったり、自家蛍光の問題のため、広く実用化しているとはいえません。当研究室では10色以上のマルチカラー蛍光イメージングを実現することを目指し、特にリニアアンミキシングにおける上記の問題点を克服する新規マルチカラーイメージング法の開発を行っています。